Maulwürfe: intersexuell und genetisch gedopt
Vervielfachungen und Inversionen von DNA-Abschnitten führen zur Vermännlichung von Maulwurf-Weibchen
Weibliche Maulwürfe besitzen neben Eierstock- auch Hodengewebe, das männliche Geschlechtshormone produziert – was sie von der Kategorisierung in zwei Geschlechter abweichen lässt. Welche Erbgut-Umbauten zu dieser einzigartigen Entwicklung beitragen, beschreibt ein Team um die Berliner Forscher Stefan Mundlos und Darío Lupiáñez in Science.
Maulwürfe sind besondere Geschöpfe, die sich in einem extremen Lebensraum tummeln. Als Bergarbeiter tief in der Erde besitzen sie einen zusätzlichen Finger an jeder Vorderpfote und eine außergewöhnlich starke Muskulatur. Zudem sind Maulwurf-Weibchen zweigeschlechtlich, die Tiere bleiben jedoch fruchtbar. Wie es für Säugetiere typisch ist, sind sie mit zwei X-Chromosomen ausgestattet, besitzen aber sowohl funktionierendes Eierstock- als auch Hodengewebe. Beide Gewebetypen sind bei Maulwürfen in einem Organ, den Ovotestes, vereint – und das ist einzigartig unter Säugetieren.
Viel Testosteron im Blut der Maulwurf-Weibchen

Das Hodengewebe der Maulwurf-Weibchen produziert zwar keine Spermien, wohl aber große Mengen des Geschlechtshormons Testosteron, sodass die Weibchen ähnlich hohe Werte wie die Männchen aufweisen. Vermutlich macht dieses natürliche „Doping“ die Maulwurf-Weibchen aggressiv und muskulös, was für ein Leben unter der Erde von Vorteil ist, wo sie Höhlen graben und um Ressourcen kämpfen müssen.
In einer Studie im Fachjournal Science berichten Berliner Wissenschaftlerinnen und Wissenschaftler nun von den genetischen Besonderheiten, die zu der charakteristischen sexuellen Entwicklung bei Maulwürfen führen. Demnach sind es vor allem Veränderungen in der Struktur des Genoms, die zu einer veränderten Steuerung der Gen-Aktivität führen. Dies kurbelt in den Weibchen neben dem genetischen Programm für die Hodenentwicklung auch die Enzyme für die Produktion männlicher Hormone an.
Die Studie eines internationalen Teams entstand unter der Leitung von Professor Stefan Mundlos, Forschungsgruppenleiter am Max-Planck-Institut für molekulare Genetik (MPIMG) und Direktor des Instituts für Medizinische Genetik und Humangenetik der Charité – Universitätsmedizin Berlin sowie Dr. Darío Lupiáñez, Forschungsgruppenleiter am Berlin Institute for Medical Systems Biology (BIMSB), das zum Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) gehört.
Genomische Mechanismen der Evolution
„Seit Darwin gilt, dass die unterschiedlichen Erscheinungsbilder von Lebewesen durch graduelle Veränderungen im Erbgut entstanden, die an die nächsten Generationen weitergegeben wurden“, sagt Mundlos. „Aber wie hängen DNA-Veränderungen und Ausprägung konkret zusammen und wie findet man sie?“
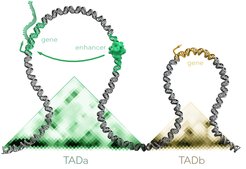
Um dieser Frage nachzugehen, sequenzierten die Forscherinnen und Forscher das Genom des Iberischen Maulwurfs (Talpa occidentalis) erstmals komplett. Auch die dreidimensionale Struktur des Erbgutes in der Zelle untersuchten sie. Denn im Zellkern bilden Gene und zugehörige Steuersequenzen regulatorische Domänen – das sind relativ isolierte „Nachbarschaften“, in denen DNA-Abschnitte besonders häufig miteinander interagieren. „Unsere Hypothese war, dass beim Maulwurf nicht nur Veränderungen in den Genen, sondern vor allem auch in der Regulation dieser Gene existieren“, sagt Mundlos.
Im Laufe der Maulwurf-Evolution hätten sich demnach nicht nur einzelne DNA-Buchstaben geändert, sondern sich auch größere Teilstücke des Genoms verlagert, sagt der Forscher. Gelangen DNA-Abschnitte von einer Stelle an die nächste, können ganz neue regulatorische Domänen entstehen und damit neue Gene aktivieren oder vorhandene verstärken oder abschwächen.
Programm zur Hodenentwicklung aktiviert
„Die sexuelle Entwicklung von Säugetieren ist komplex, aber wir haben eine recht gute Vorstellung davon, wie der Prozess abläuft“, sagt Darío Lupiáñez. „Ab einem bestimmten Zeitpunkt geht die Entwicklung in die eine oder andere Richtung weiter, männlich oder weiblich. Wir wollten wissen, wie die Evolution diesen eigentlich festgelegten Ablauf moduliert und die intersexuellen Eigenschaften von Maulwürfen ermöglicht.“
Tatsächlich entdeckte das Team beim Vergleich mit dem Genom anderer Tiere und des Menschens eine Inversion – also einen umgedrehten Erbgutabschnitt – in einem Bereich, der an der Bildung der Hoden beteiligt ist. Durch die Drehung geraten zusätzliche DNA-Abschnitte in die regulatorische Domäne des Gens FGF9, was die Steuerung und Regulation des Gens neu organisiert. „Diese Veränderung führt dazu, dass sich in weiblichen Maulwürfen neben Eierstock- auch Hodengewebe entwickeln kann“, erklärt die Erstautorin der Studie Dr. Francisca Martinez Real, Wissenschaftlerin am MPIMG und am Institut für Medizinische Genetik und Humangenetik der Charité.
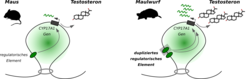
Zusätzlich stieß das Team auf eine Verdreifachung eines Genom-Abschnitts um das Gen CYP17A1, das für die Produktion männlicher Sexualhormone (Androgene) zuständig ist. „Durch die Triplikation entstehen zusätzliche Steuersequenzen für das Gen – und in den Ovotestes der Maulwurf-Weibchen werden verstärkt männliche Geschlechtshormone hergestellt, vor allem mehr Testosteron“, sagt Real.
Wilde Maulwürfe und transgene Mäuse
Eine Herausforderung der Studie war es, dass sich die sehr territorialen Maulwürfe nicht im Labor halten lassen. „Wir mussten sämtliche Untersuchungen an wildlebenden Maulwürfen vornehmen“, sagt Lupiáñez. Er und Real waren monatelang in Südspanien unterwegs und sammelten Proben für ihre Experimente. „Diese Schwierigkeit war allerdings zugleich eine Stärke unserer Studie. Unsere Ergebnisse gelten nicht nur für Labortiere, sondern auch für freilebende Tiere.“
Die beiden Genomveränderungen tragen tatsächlich zur besonderen Sexualität von Maulwurf-Weibchen bei. Dies wies die Forschungsgruppe nach, indem sie die genetischen Veränderungen aus den Maulwürfen im Mausmodell nachahmte. Die weiblichen Mäuse hatten erhöhte Androgenspiegel, die so hoch waren wie bei normalen Mäuse-Männchen. Sie waren außerdem deutlich kräftiger als unveränderte Artgenossinnen.
Evolution bedient sich im genetischen Werkzeugkasten
Bei Maulwürfen sind die Geschlechter nicht klar voneinander abgegrenzt, vielmehr bewegen sich die Weibchen auf einem Spektrum zwischen typisch weiblicher und typisch männlicher Ausprägung, sie sind also intersexuell.
„Unsere Befunde sind ein gutes Beispiel dafür, wie bedeutend die dreidimensionale Organisation des Genoms für die Evolution ist“, sagt Lupiáñez. „Die Natur bedient sich aus dem vorhandenen Werkzeugkasten der Entwicklungsgene und ordnet sie nur neu an, um ein Merkmal wie die Intersexualität zu erzeugen. Andere Organsysteme und die Entwicklung werden dabei nicht beeinträchtigt.“
„Historisch gesehen hat der Begriff Intersexualität erhebliche Kontroversen ausgelöst“, sagt Mundlos. „Es gab und gibt die Tendenz, intersexuelle Phänotypen als krankhafte Zustände zu charakterisieren. Unsere Studie zeigt, wie komplex die sexuelle Entwicklung ist und dass die Natur ein großes Spektrum an Zwischentypen hervorbringen kann.“
Gemeinsame Pressemitteilung des Max-Planck-Instituts für molekulare Genetik, der Charité – Universitätsmedizin Berlin und des Max-Delbrück-Centrums für Molekulare Medizin
Das Max-Planck-Institut für molekulare Genetik (MPIMG) befasst sich mit der Untersuchung der Funktion und Kontrolle des Genoms – insbesondere bei der Embryonalentwicklung, bei Differenzierungsprozessen, der Organentwicklung und der Entstehung von Krankheiten. Gene und Genome werden mit automatisierten Verfahren, Hochdurchsatz-Technologien und verschiedenen Modellsystemen untersucht. Zur Auswertung und Interpretation der Daten dienen bioinformatische Methoden. Die enge Verbindung von Experiment und Bioinformatik ist typisch für die Arbeit des MPIMG. In dem 1964 in Berlin-Dahlem gegründeten Forschungsinstitut arbeiten ungefähr 350 Personen und pflegen eine Kultur der Interdisziplinarität und Innovation. www.molgen.mpg.de
Die Charité – Universitätsmedizin Berlin ist mit rund 100 Kliniken und Instituten an 4 Campi sowie 3.001 Betten eine der größten Universitätskliniken Europas. Forschung, Lehre und Krankenversorgung sind hier eng miteinander vernetzt. Mit Charité-weit durchschnittlich rund 15.500 und konzernweit 18.700 Beschäftigten aus über 100 Nationen gehört die Berliner Universitätsmedizin zu den größten Arbeitgeberinnen der Hauptstadt. Dabei waren 4.553 der Beschäftigten im Pflegebereich und 4.454 im wissenschaftlichen und ärztlichen Bereich tätig. An der Charité wurden im vergangenen Jahr 154.261 voll- und teilstationäre Fälle sowie 700.819 ambulante Fälle behandelt. Im Jahr 2019 hat die Charité Gesamteinnahmen von rund 2,0 Milliarden Euro, inklusive Drittmitteleinnahmen und Investitionszuschüssen erzielt. Mit den 179,1 Millionen Euro eingeworbenen Drittmitteln erreichte die Charité einen erneuten Rekord. An der medizinischen Fakultät, die zu den größten in Deutschland gehört, werden mehr als 8.000 Studierende in Humanmedizin, Zahnmedizin sowie Gesundheitswissenschaften ausgebildet. Darüber hinaus gibt es 644 Ausbildungsplätze in 9 Gesundheitsberufen. www.charite.de
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) wurde 1992 in Berlin gegründet. Es ist nach dem deutsch-amerikanischen Physiker Max Delbrück benannt, dem 1969 der Nobelpreis für Physiologie und Medizin verliehen wurde. Aufgabe des MDC ist die Erforschung molekularer Mechanismen, um die Ursachen von Krankheiten zu verstehen und sie besser zu diagnostizieren, verhüten und wirksam bekämpfen zu können. Dabei kooperiert das MDC mit der Charité – Universitätsmedizin Berlin und dem Berlin Institute of Health (BIH) sowie mit nationalen Partnern, z.B. dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DHZK), und zahlreichen internationalen Forschungseinrichtungen. Am MDC arbeiten mehr als 1.600 Beschäftigte und Gäste aus nahezu 60 Ländern; davon sind fast 1.300 in der Wissenschaft tätig. Es wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Berlin finanziert und ist Mitglied in der Helmholtz-Gemeinschaft deutscher Forschungszentren. www.mdc-berlin.de














