Epigenetische Möglichkeiten und Notwendigkeiten
Forschungsbericht (importiert) 2016 - Max-Planck-Institut für molekulare Genetik
Epigenetik
Die DNA ist der Träger der Erbinformation, der Gene. Die Abfolge der Basen Adenin, Cytosin, Guanin und Thymin - die DNA-Sequenz - bildet das Fundament dafür, dass der Mensch ein Mensch und die Fruchtfliege eine Fruchtfliege ist und birgt damit auch diejenigen Merkmale, die Mutter und Vater an ihre Nachkommen vererben.
Das humane Genom ist seit 2003 bekannt [1] und die vollständige Sequenzinformation, so die Erwartung, müsste viele Fragen beantworten, wie unsere Zellen funktionieren. Da aber jede unserer Zellen mit demselben Genom ausgestattet ist, war den Wissenschaftlerinnen und Wissenschaftlern bewusst, dass die Sequenzinformation allein nicht die zum Teil sehr verschiedenen Funktionen unserer Zellen erklären kann. Eine der naheliegenden Annahmen war, dass Zellen nur jeweils einen Teil des Genoms abrufen, das heißt, nicht sämtliche Gene exprimieren.
Ein noch junger Zweig der Lebenswissenschaften wird als Epigenetik bezeichnet; er widmet sich unter anderem denjenigen Mechanismen, die es Zellen ermöglichen, nur eine klar umgrenzte Teilmenge der Gene zu verwenden. Epigenetik steht „über“ (epi) der Genetik - der Lehre der Vererbung. Epigenetische Mechanismen umfassen Regelkreise, die, je nach Kontext, verschiedene, aber stabile Zustände annehmen. Ein Beispiel ist die sogenannte Autoregulation, bei der das Produkt eines Genes seine eigene Produktion antreibt. Das betreffende Gen kann durch einen beliebigen Mechanismus eingeschaltet werden, seine Produktion aber kann, unabhängig von dem Einschaltmechanismus, aufrechterhalten werden.
Epigenetik bedeutet aber noch mehr als autoregulatorische Mechanismen. Die neue Lehre umfasst auch die Vererbung des zellulären Zustands an die Tochterzellen nach einer mitotischen Teilung. Dies geschieht einerseits durch die Verteilung von Genprodukten auf die Tochterzellen, was die autoregulatorischen Regelkreise wieder anwirft. Andererseits werden Informationen „über“ der DNA-Sequenz gespeichert, die an die Tochterzellen weitergegeben werden können. Diese zusätzliche Information ist in Veränderungen des Chromatins abgelegt, sozusagen über der Nukleotidsequenz. Chromatin besteht hauptsächlich aus DNA und Histon-Proteinen. DNA und Histone können chemisch modifiziert werden, ohne dass die DNA-Sequenz dadurch verändert wird. Bestimmte Modifikationen werden als „Kurzzeitgedächtnis“ für den Ablauf von biochemischen Prozessen, wie der Transkription von RNA, verwendet. Andere dienen als „Langzeitgedächtnis“, das über mehrere Zellgenerationen hinweg stabil ist.
Epigenetische Möglichkeiten
Das epigenetische Langzeitgedächtnis wird von Chromatin-Modifikationen gebildet, die nicht benötigte Gene abschalten. Diese Gene werden bereits während der Differenzierung der Zellen ausgewählt. Die Entwicklung eines Organismus beginnt stets mit Zellen, die noch alle Zelltypen des Organismus bilden können. Interessanterweise tragen in diesem noch ursprünglichen Zelltyp aber bereits viele Gene eine bestimmte Kombination von Chromatin-Modifikationen. Diese Kombination ist auffallend, denn eine der Chromatin-Modifikationen spiegelt transkriptionelle Aktivität wider, die andere aber transkriptionelle Repression [2]. Die Entdeckung dieser widersprüchlichen Kombination ließ annehmen, dass die Gene auf diese Weise auf eine spätere Aktivität vorbereitet werden, nicht zuletzt deswegen, weil viele dieser derart markierten Gene an Differenzierungsprozessen beteiligt sind. In diesem Zusammenhang vermutet man, dass epigenetische Veränderungen des Chromatins nicht nur vergangene Entscheidungen, sondern auch erst in der Zukunft liegende Regulations-Möglichkeiten darstellen.
Da eine aktivierende und eine repressive Chromatin-Modifikation allerdings nie gleichzeitig an ein und demselben Gen gemessen wurden, wurde das reale Vorhandensein der Kombination beider Modifikationen angezweifelt. Um diese Zweifel auszuräumen, wurde am Institut ein Verfahren entwickelt, zwei Chromatin-Modifikationen gleichzeitig zu messen. Dieses Verfahren wurde auf humane T-Gedächtniszellen angewandt. T-Gedächtniszellen haben nur noch ein eingeschränktes Entwicklungspotential, müssen aber im Falle einer Infektion sehr schnell eine Immunantwort auslösen. Daher sollten auch hier Gene für eine schnelle Aktivierung vorbereitet sein.
Die Ergebnisse dieser Messung zeigen, dass die Kombination aus aktivierenden und repressiven Chromatin-Modifikationen tatsächlich in T-Gedächtniszellen vorkommt. Allerdings sind die so markierten Gene nicht an der Immunantwort, sondern, wie bei den Zellen der frühen Embryonalentwicklung, an Differenzierungsprozessen beteiligt [3]. Dieses Ergebnis ist daher nur schwer mit der Idee in Einklang zu bringen, dass die Kombination aus aktivierenden und repressiven Chromatin-Modifikationen Gene auf eine spätere Aktivität vorbereitet.
Epigenetische Notwendigkeiten
Wenn diese Kombination also nicht die zukünftigen Entscheidungs-Möglichkeiten einer Zelle widerspiegelt, wozu ist sie dann notwendig? Eine Antwort liefert der mit dieser Chromatin-Kombination markierte DNA-Abschnitt: Dessen Sequenz enthält weitaus häufiger ein Cytosin, gefolgt von einem Guanin, als der Rest des Genoms. Genau diese Basenabfolge wird durch Enzyme erkannt, die das Cytosin chemisch modifizieren. Das modifizierte Cytosin jedoch zerfällt leicht zu Thymin, während unverändertes Cytosin zu Uracil zerfallen kann, das natürlicherweise nicht in DNA, sondern nur in RNA vorkommt. Daher wird Uracil sofort durch Reparaturmechanismen erkannt und durch ein Cytosin ersetzt. Das Thymin allerdings wird nicht erkannt, was zu einem Basenaustausch und damit zu einer Mutation führen kann. Dementsprechend hoch ist die Mutationsrate von einem Cytosin zu einem Thymin im Kontext der Basenabfolge Cytosin-Guanin, was zu einem Verlust der Basenabfolge Cytosin-Guanin im menschlichen Genom geführt hat. Sogar der genetische Code ist direkt von diesem Verlust betroffen, so werden Codons, die die Basenabfolge Cytosin-Guanin beinhalten, wesentlich seltener verwendet.
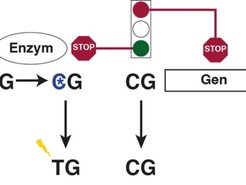
In einigen wenigen Bereichen des Genoms kommt diese Basenabfolge öfter vor, und es sind genau diese Bereiche, die von der aktivierenden Chromatin-Modifikation markiert werden. Dazu erkennen bestimmte Enzyme zuerst die unveränderte Basenabfolge Cytosin-Guanin und katalysieren nachfolgend,die aktivierende Chromatin-Modifikation. Kommt die aktivierende Chromatin-Modifikation alleine vor, so ist das Gen aktiv. Kommt sie jedoch in Kombination mit der repressiven Chromatin-Modifikation vor, so ist das Gen inaktiv. Die aktivierende Chromatin-Modifikation behindert diejenigen Enzyme, die Cytosin chemisch verändern [4], und dementsprechend tragen die so markierten DNA-Bereiche auch keine Cytosin-Modifikation (Abb. 1).
Daher ist die Markierung mit der Kombination aus einer aktivierenden und einer repressiven Chromatin-Modifikation die Standardantwort auf DNA-Sequenzen, die viele unveränderte Cytosine-Guanine Basenabfolgen enthalten [5]. Dieser Zustand ist während der Lebensspanne eines Organismus und in der Keimbahn stabil. So werden wichtige Gene vor Mutationen geschützt, die einerseits für die eigene Embryonalentwicklung, anderseits aber auch für die Embryonalentwicklung der Nachkommen notwendig sind. Die Kombination aus einer aktivierenden und repressiven Chromatin-Modifikation stellt daher nicht epigenetische Möglichkeiten dar, sondern ist notwendig, um wichtige Gene während der eigenen Lebensspanne und die der Nachkommen vor Mutationen zu schützen. Chromatin-Modifikationen beeinflussen die DNA Sequenz und spielen genau deswegen eine wichtige Rolle in der Evolution.
